iPS細胞の再生医療2製品を実用化へ
厚労省部会が了承、世界初
<< Return to Main
-
Nikkei Online, 2026年2月19日 19:11更新
厚生労働省の専門部会は19日、iPS細胞を使った再生医療2製品の製造販売を了承した。重い心不全、症状が進んだパーキンソン病の治療に用いる。iPS細胞製品の実用化は世界初となる。京都大学の山中伸弥教授が2006年に世界に先駆けマウスiPS細胞の作製に成功してから20年、いよいよ実用段階に入る。
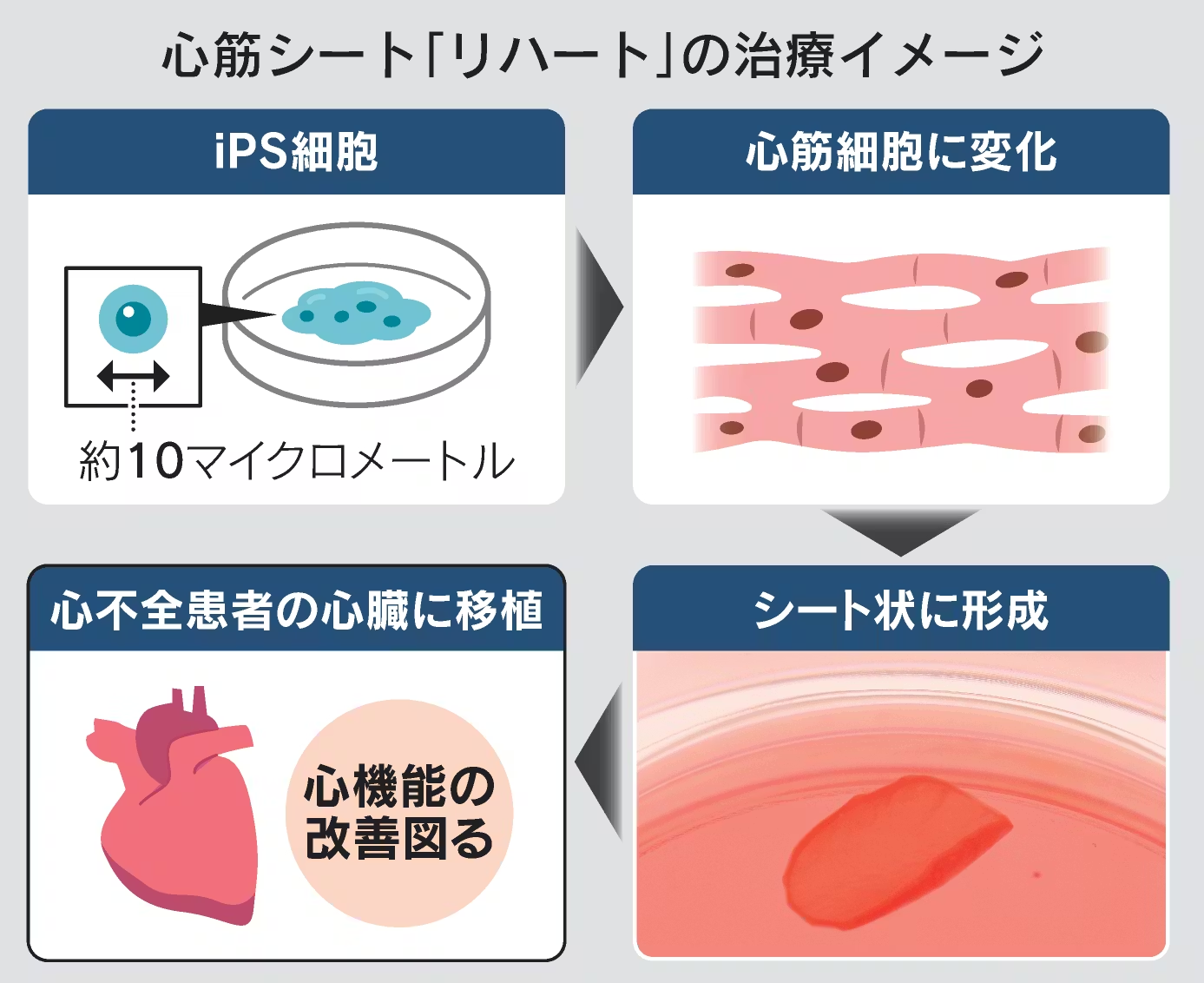
大阪大学発のスタートアップ、クオリプスの心不全向け心筋細胞シート「リハート」と住友ファーマのパーキンソン病向け治療薬候補「アムシェプリ」について、薬事審議会(厚労相の諮問機関)の再生医療等製品・生物由来技術部会が了承した。
いずれの製品も患者にいち早く届けるために安全性を確認したうえで有効性が推定できる段階で暫定的に販売できる条件・期限付き承認となる。7年以内に有効性や安全性を検証し、再度承認を申請する必要がある。
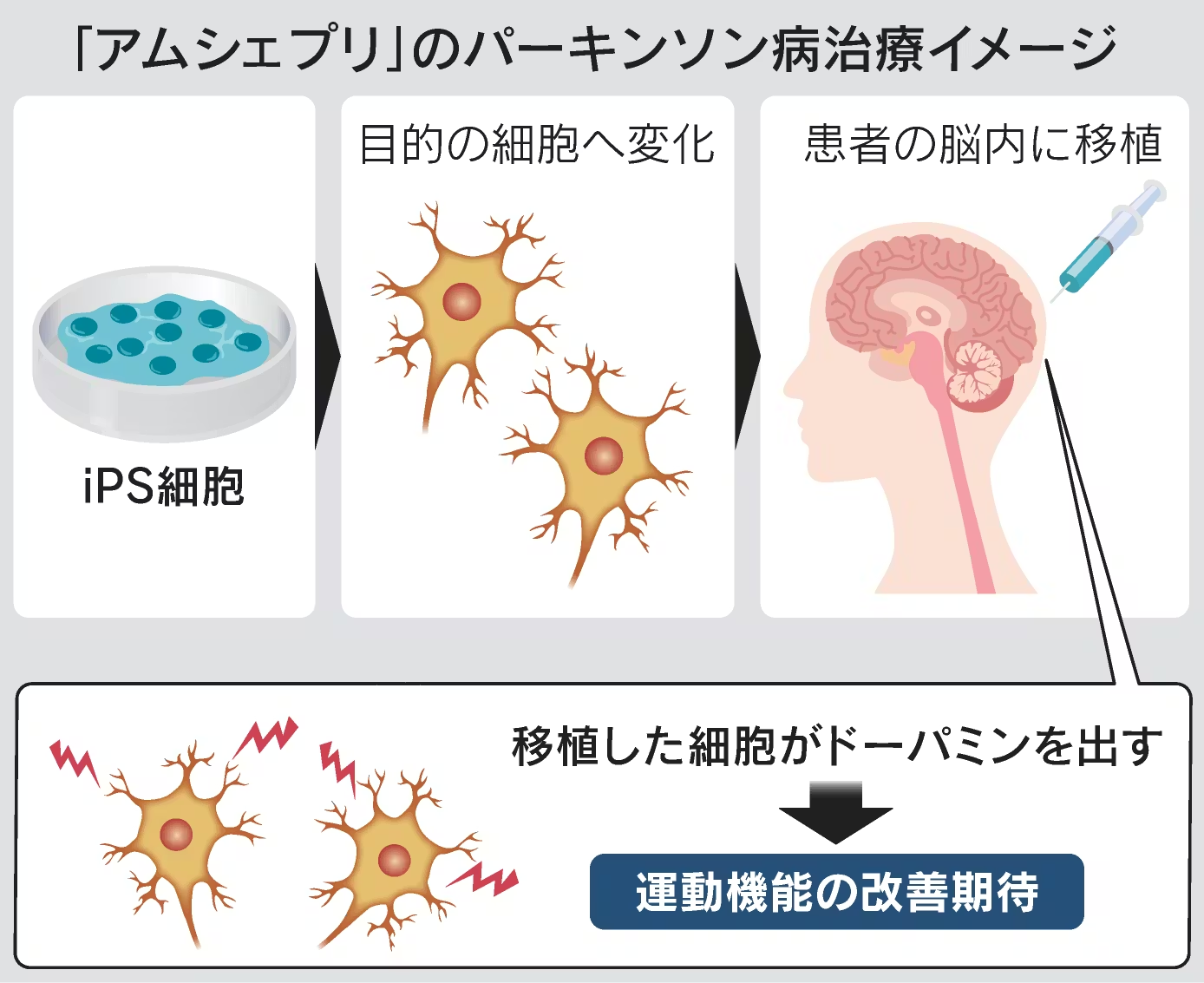
今後は必要な手続きを経て上野賢一郎厚労相が承認する。過去の例では1〜2カ月程度で承認することが多い。その後、中央社会保険医療協議会(厚労相の諮問機関)が公的医療保険で使う際の価格を決める。
クオリプスのリハートは他人のiPS細胞からつくった心筋細胞をシート状にした製品だ。薬などによる治療で効果が不十分な重症の心不全患者に使う。
住友ファーマのアムシェプリはパーキンソン病患者で不足する神経伝達物質ドーパミンを出す神経細胞のもとになる細胞を脳に注入する。神経細胞からドーパミンが出ることで患者の運動機能を改善する効果が期待される。同社は米国でも臨床試験を進めている。
山中教授は「医療として確立するには、ここからさらに多くの症例で安全性と有効性を確かめるプロセスが不可欠。浮足立つことなく、科学的な慎重さを持って、引き続き一歩ずつ着実に進んでいくことが重要だ」とコメントした。